Химики из Оксфорда разработали новый тип катализатора. Для этого они присоединили два фермента-оксидоредуктазы к микроскопической чешуйке графита. Исследователи отмечают, что такая система может быть настроена для катализа широкого круга реакций.
Фрейзер Армстронг (Fraser Armstrong) с соавторами присоединили к графиту гидрогеназу и нитрат-редуктазу. При суспендировании полученных частиц в растворе, содержащем нитрат-ионы, через который продували водород, электроны, оторванные от водорода, перемещаются к редуктазе по участку графита, восстанавливая нитрат в нитрит.
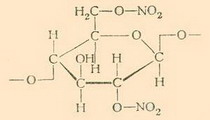
Окисление водорода при посредстве гидрогеназы (зеленый цвет на схеме) поставляет электроны для каталитического восстановления при участии второго фермента (пурпурный цвет на схеме) (Рисунок из Nature Chem. Biol., 2007, DOI: 10.1038/nchembio.2007.47)
Армстронг отмечет, что результаты исследования являются ярким примером доказательства новой концепции использования ферментов для катализа. Было продемонстрировано, что возможно использовать водород в качестве простого источника электронов для фрагмента графита; в этом случае электроны передаются второму ферменту и используются для переработки специфических субстратов. Использование «связанных ферментных пар» имеет широкий синтетический потенциал для многих каталитических реакций.
Реакция не протекает в отсутствие графита, что демонстрирует необходимость использования этого «посредника» для переноса электронов от одного фермента к другому. Нитрат-редуктаза была заменена на фумарат-редуктазу, и эксперимент был воспроизведен. При этом наблюдалось восстановление фумарата в сукцинат.
Стефан Чапмен (Stephen Chapman) из Университета Эдинбурга подчеркивает изящность работы. По его мнению, особенно интересной чертой работы демонстрацию необходимости использования графита как медиатора переноса электронов между катализаторами.